脳の働きに必要なカルシウムチャネルを阻害して、制御する新しい仕組みを、理化学研究所脳科学総合研究センターの御子柴克彦(みこしば かつひこ)チームリーダーと濱田耕造(はまだ こうぞう)研究員らが発見した。認知症など脳の病気の発症原因を探るのにも役立つ成果として期待される。9月8日の米科学アカデミー紀要オンライン版に発表した。
このカルシウムチャネルはイノシトール3リン酸(IP3)受容体。細胞内の小器官である小胞体の膜上に局在するタンパク質で、神経伝達や記憶・学習を担っている。この受容体は4つサブユニットが組み合わさって、中心部にカルシウムイオンを1つだけ通す小さなイオン透過口を形成し、カルシウムチャネルとして働く。
脳の神経細胞に信号が伝わると、細胞膜からIP3が切り出され、細胞内に遊離してIP3受容体に結合する。IP3が結合すると、チャネルの構造が変化して、小胞体からカルシウムイオンが細胞内にどっと放出され、記憶や学習などに必要なさまざまな生化学反応が起こす。この立体構造(アロステリック)変化に不具合があると、脳の機能に障害が発生すると考えられている。しかし、その制御の詳細はまだ謎だった。
研究グループは、IP3受容体に作用して立体構造変化を阻害する酵素として、トランスグルタミナーゼを見いだした。神経細胞やグリア細胞に存在する2型トランスグルタミナーゼが、IP3受容体の立体構造の変化を阻害してカルシウムの放出口を閉じる3通りの仕組みを細胞実験などで詳しく確かめた。さらに、この制御が細胞内のオートファジー(自食作用)の調節に関与することも明らかにした。
トランスグルタミナーゼは、アルツハイマー病やハンチントン病など神経変性疾患の脳で活性化されることが知られている。研究グループは、ハンチントン病患者のリンパ球やモデルマウスを用いた実験で、IP3受容体の立体構造変化の阻害がハンチントン病に関与する可能性を示した。認知症の原因となる脳神経変性疾患では、カルシウムシグナルの制御異常が報告されており、認知症研究の新しい手がかりとしても注目される。
御子柴克彦チームリーダーは「IP3受容体の立体構造変化を阻害する酵素を必死に探したところ、その正体はトランスグルタミナーゼだった。この発見によって、IP3受容体が阻害される分子レベルの仕組みが明らかになった。アルツハイマー病やパーキンソン病など多くの脳神経変性疾患で、IP3受容体の活性が落ちていることが最近わかってきた。脳神経変性疾患の基本的な原理の可能性もあり、それを解明する一歩としても、研究を発展させたい」と話している。
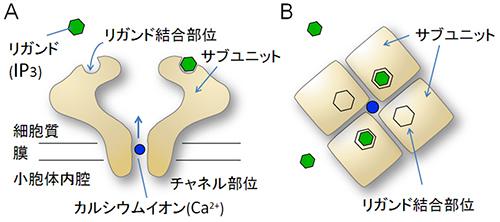
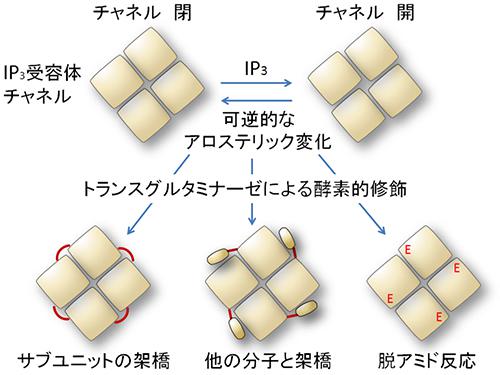
(いずれも提供:理化学研究所)
関連リンク


