筋肉が次第に動かなくなる難病の筋萎縮性側索硬化症(ALS)のモデルマウスに、ヒトの人工多能性幹細胞(iPS細胞)由来のグリア系神経前駆細胞を移植して、生存期間を延ばすのに、京都大学iPS細胞研究所の近藤孝之研究員と井上治久教授らが成功した。iPS細胞の臨床応用の可能性を探る成果の一つといえる。京都大学の山中伸弥iPS細胞研究所所長、医学研究科の高橋良輔教授、慶應義塾大学医学部の岡野栄之教授、中村雅也准教授らとの共同研究で、6月26日付の米科学誌 Stem Cell Reports オンライン版に発表した。
遺伝子(SOD1)の変異によるALSモデルマウスに、マウスかヒト胎児由来の神経前駆細胞を移植すれば、運動神経細胞の変性や病態の進行が緩和することは知られている。しかし、臨床で応用するには、持続的に供給が可能であるヒトの細胞で研究する必要があった。iPS細胞なら、原理的にはこの問題を解決できる。
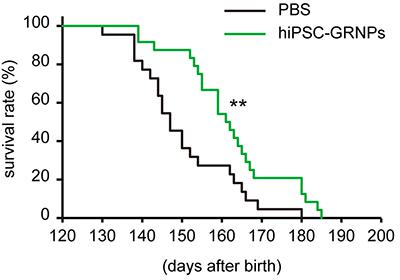
井上治久教授らの研究グループは、ヒトiPS細胞からグリア系神経前駆細胞を誘導し、その細胞8万個を生後90日のALSマウスモデルの腰髄に移植した。実験はそれぞれ24匹(雄17匹、雌7匹)で実施し、生後何日まで生き延びるのかを比較した。移植されたマウスの平均生存日数は生後162日で、移植されていないマウスの150日より13日、8%長くなった。
細胞移植後50〜80日目のマウスで調べると、移植された細胞は、グリア細胞の一種で、多数の突起を持ち、神経ネットワークの構造の維持などをするアストロサイトに分化していた。iPS細胞を利用する際に懸念されている腫瘍の形成はこの実験で観察されなかった。神経栄養因子の量を調べたところ、生着した移植細胞に加え、マウスのもともとの細胞の神経栄養因子の発現量も増えていることがわかった。移植された細胞は、神経栄養因子を増加させ、脊髄環境を改善していることが示された。
研究グループは「グリア系の細胞は神経細胞の周りの環境を整える機能をもっている。本来機能させるべき運動神経細胞を花に例えると、その花を咲かせるために必要な栄養分を供給する土の役割をする細胞だ。失われた運動神経細胞の再生は難しいので、今回は、iPS細胞から作った良い土を補った。今後は、iPS細胞から誘導した運動神経細胞と一緒に移植して効果を研究したいが、実際にヒトで試験するまでには課題はまだ多い」としている。