人が恒常性を維持する原理の一端が解けた。上皮細胞間のすき間を密着させてバリアとなっている分子の構造を、名古屋大学細胞生理学研究センターの藤吉好則(ふじよし よしのり)特任教授、東京大学大学院理学系研究科の濡木理(ぬれき おさむ)教授、大阪大学大学院生命機能研究科の月田早智子(つきた さちこ)教授らが世界で初めて解明した。
上皮細胞間接着の膜タンパク質、クローディンの構造を突き止めたもので、体表面や器官表面の細胞間をシールして、多細胞の生命体を維持している実体がわかったといえる。心筋梗塞や不整脈などクローディンが関わる多くの病気の治療に道を開く成果としても注目される。4月18日発行の米科学誌サイエンスに発表した。
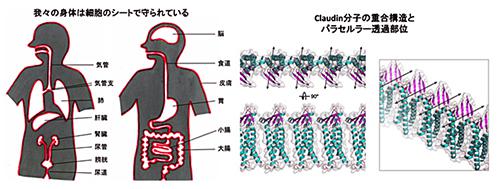
われわれの体の恒常性は、体表面や器官表面にあるシート状の上皮細胞で守られている。シートを形成する上皮細胞間のすき間を密着させている主役のタンパク質は1998年、京都大学教授だった故月田承一郎さんらによって同定され、クローディンと名付けられた。クローディンはこれまでヒトやマウスで27種類が確認されており、組織ごとに異なるタイプのクローディンが発現することで、器官特異的なバリアが形成されると考えられている。しかし、この分子がどのような形をして重合しているか、わかっていなかった。
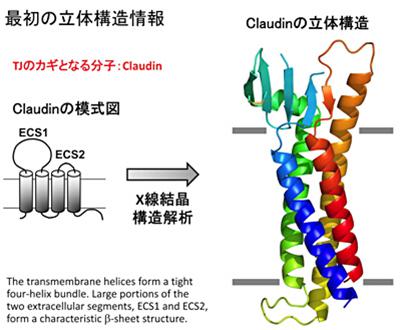
研究グループはマウスのクローディンを特殊な脂質環境中で結晶化し、大型放射光施設SPring-8(兵庫県佐用町)のX線マイクロビームで解析した。その結晶は幅3ナノメートルの分子で、4回膜貫通型という新規の折りたたみ構造だった。細胞の外側には、手のひらのように、指に当たる5つのβシートからなるループ構造が出ていた。その手のひらがイオンを選択的に透過しうることもわかった。クローディンの種類ごとに類似性を計算すると、よく似た構造をとっていると予想できた。
さらに、クローディンは同じ向きで横一列の数珠つなぎに並ぶ構造を取っていることも、初めて明らかにした。研究グループは「隣接する細胞間では、ベルト状に連なったクローディン同士が手のひらを向かい合わせて結合している。その距離や形状、電荷的な環境によって、細胞間隙にイオンや小分子を通したり、通さなかったりする制御が可能になっている」とみている。
研究グループの藤吉好則さんは「クローディンは体の恒常性を保つ重要な分子だが、うねうねと重合して柔軟に曲がるので、結晶化が難しかった。6年がかりで、結晶化しやすい分子を見つけだし、その変異も利用して、ようやく構造が解析できた。上皮細胞間の接着の謎を解く重要な成果だと思う。今後は、血管脳関門にあるバリアも研究して、脳の中に薬を送り込めるようにしたい」と話している。