細胞内の小器官である小胞体が異常なタンパク質を「自家処理」する新たな仕組みを発見した、と名古屋大学などの研究グループが発表した。既知の仕組みとは異なり、タンパク質が小胞体の内部で分解される。糖尿病や各種の神経変性など、関連する疾患の治療法の開発につながる可能性があるという。
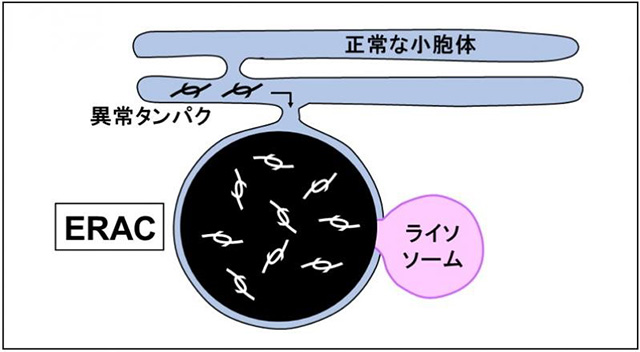
小胞体は細胞内で作られたタンパク質を正しい形に折り畳み、細胞外に出せるようにする。折り畳みに失敗した異常タンパクがたまった状態を「小胞体ストレス」といい、異常タンパクを小胞体から細胞質に出して分解する仕組みが既に知られてきた。またいくつかの疾患では、一部の小胞体内に異常タンパクが集まった区画「ERAC」ができることがこのグループの研究で分かっていたが、その働きは謎だった。
名古屋大学医学系研究科の有馬寛教授(糖尿病・内分泌内科学)らのグループは、一部の小胞体に異常タンパクが蓄積する遺伝性疾患「家族性中枢性尿崩症」を持つ実験用マウスを使用。微細な三次元構造を判別できる最新の「連続ブロック表面走査電子顕微鏡」により小胞体を詳しく観察した。
その結果、ERACが小胞体の正常な部分や、タンパク質分解酵素を含む小器官「ライソソーム」とつながっていることが判明。さらに別の顕微鏡などの分析により、異常タンパクが正常部分からERACへと送り込まれ隔離された上、ライソソームから送り込まれた酵素に分解されるという、いわば自家処理の仕組みがあることを突き止めた。

小胞体ストレスに対処する仕組みは(1)異常タンパクに目印のタンパク質がつながり、そこに酵素が駆けつけて分解する「ユビキチン−プロテアソーム系」、(2)異常タンパクを含む細胞質を膜で取り囲み、中身を分解する「オートファジー」の、2つの仕組みが知られてきた。いずれも異常タンパクを細胞質に出してから分解する。これらに対し今回発見した仕組みでは、異常タンパクを小胞体内で分解する。
ERACは、小胞体ストレスが関係する他の病気の実験動物でも見つかっている。有馬教授は「小胞体ストレス応答の普遍的なものではないか。さらに解明することで、新たな治療法の開発につながる可能性がある」と述べている。
研究グループは名古屋大学、生理学研究所、自治医科大学、岡山大学で構成。成果は7日付の米科学誌「アイサイエンス」に掲載された。
関連リンク
- 名古屋大学などプレスリリース「小胞体内における異常タンパクの新たな処理メカニズムを発見!」





