がん(悪性新生物)は、わが国で40年にわたり死因のトップを独走している。2020年には約38万人が死亡し、死因の実に3割近くを占める。高齢化で患者が増加する一方、診断や治療法の進歩などにより、生存率は改善傾向にあるといわれる。
こうした中、がん治療に大きな革新をもたらす可能性のある成果が、岡山大学の研究グループから挙がった。微生物が持ち、光を感じて細胞をアルカリ化するタンパク質を使い、狙った細胞にアポトーシス(自死)をさせる技術を開発した。実用化できれば、従来の「ネクローシス」(壊死)の方法とは根本的に異なり、副作用の起こらない治療法になるという。
光を感じるタンパク質に着目
がん治療では、がん細胞を死なせることが重要だ。その主要な手段である薬剤は、多くががん細胞だけでなく周囲の正常な細胞にも作用し、副作用を起こす問題があった。光を使った治療としてはこれまで、がん細胞に薬剤を集め、光を当てて殺すいくつかの方法が見いだされてきた。中でも光免疫療法は、免疫の仕組みも巧みに利用する画期的な治療法として近年、注目されている。
一方、岡山大学学術研究院医歯薬学域(薬学系)の須藤雄気教授(生物物理学)は「これらはいずれも化学物質を使い、活性酸素や熱で物理的にネクローシスを起こす方法。改良が進むにせよ、副作用をなくせない」と指摘する。
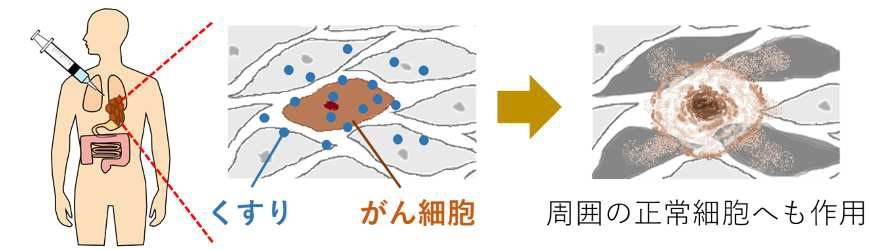
細胞の死に方には、大きく分けて2通りある。けがや毒、ウイルス感染などによって細胞が傷ついて死ぬネクローシスと、生き物の体を維持するため不要な細胞を積極的に死なせるアポトーシスだ。「化学物質ではなくタンパク質を使い、目的のがん細胞にひっそりとアポトーシスをさせられれば、副作用のない画期的ながん治療を実現できるのではないかと考えた」(須藤教授)。
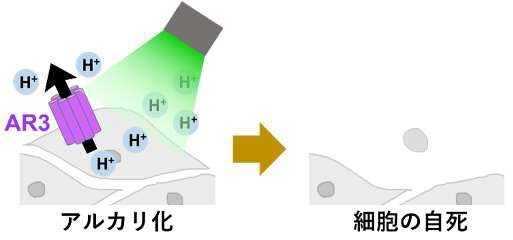
そこで須藤教授の研究グループは、米国の塩湖に生息する微生物が持ち、光によって働く物質「アーキロドプシン3(AR3)」に着目した。タンパク質「ロドプシン」には光を吸収する性質があり、例えばヒトなどの脊椎動物では、目の中で視覚を担っている。AR3はその一種で、細胞の外へ水素イオンを運び出し、細胞内の水素イオン濃度を下げる性質を持つ。水素イオン濃度が低い状態は、アルカリ性である。また、細胞のアルカリ化はアポトーシスの引き金になる。こうしたことから「細胞内をAR3でアルカリ化すれば、細胞のアポトーシスに影響を与えられるのでは」と考え、実験に挑んだ。
従来と根本的に違う、画期的な治療法へ
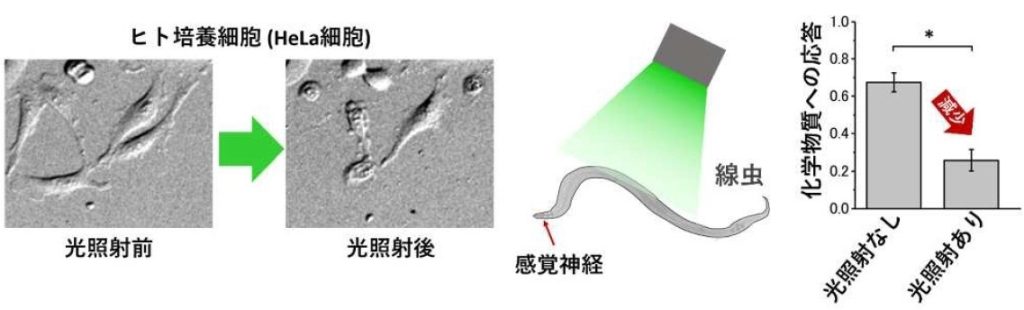
まず、ヒトのがん由来の細胞にAR3を合成させ、波長550ナノメートル(ナノは10億分の1)ほどの緑色の光を当てた。すると、AR3の働きで細胞の中がアルカリ化され、3時間程度でほとんどの細胞がアポトーシスに至った。
次に、生きた動物で確かめた。実験動物としてよく使われる線虫の感覚神経細胞にだけAR3を合成させた後、全身に緑色の光を当てると、感覚神経細胞の化学物質への応答が低下した。感覚神経細胞で、AR3によって水素イオンが細胞の外へと汲み出され、細胞がアルカリ化して死んだとみられる。これらの結果から、AR3と光を使うことで、狙った細胞にアポトーシスが起きることを突き止めた。
なお、細胞にAR3を合成させるには、細胞にAR3の遺伝子を注入する。新型コロナウイルス感染症(COVID-19)のmRNA(メッセンジャーRNA)ワクチンが、細胞内にmRNAを入れてタンパク質を合成させる仕組みに似ている。遺伝情報の目印を手掛かりに、狙った細胞だけにAR3を合成させられるという。
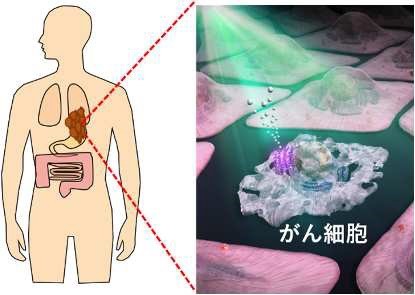
須藤教授は「ヒトのがん細胞でAR3を作り、今回開発した『光細胞死滅法』を使うと、がん細胞だけを死滅させ、周囲の正常な細胞には副作用が起きない。『光でがんを殺すのだから、従来法と同じでは』と言われることもあるが、ネクローシスではなくアポトーシスであり根本的に違う。画期的な治療法につながる」と説明する。
研究グループは須藤教授、岡山大学学術研究院医歯薬学域(薬学系)の小島慧一(けいいち)助教らで構成。成果は米国化学会誌の電子版に2月17日に掲載された。研究は科学技術振興機構(JST) 戦略的創造研究推進事業、文部科学省科学研究補助金などの支援を受けている。
先生の話を信じなかった学生、お手柄
ヒトの細胞と、比較的単純な実験動物で効果を確かめたことから、次はマウスなどの哺乳類の組織で実験を進める。続いてヒトのがん組織、さらに実際の患者の組織へと検証を進める方針だ。
実は今回の成果は、学生の秘策が鍵となった。須藤教授に黙って、細胞に与えるpH(水素イオン濃度指数=酸性・中性・アルカリ性の指標)の条件を変えた実験を並行していたという。須藤教授は「私はこの実験は、中性では絶対できないと思っていた。『細胞をアルカリ液に漬けたら死ぬが、AR3により加速するかどうか』などと考え、(アルカリ性の)pH9で実験させた。しかし彼は(中性の)pH7、つまり体内で起こり得る条件でもやっていた」。

中性では長時間にわたり光を当て、観察を続ける必要がある。「短時間では『中性では起こらないね』で終わってしまうところ、彼は根気よく3時間、4時間と実験した。中性で起こるのなら、治療に使える可能性がある。指導者の話を良い意味で信じず、学生によってブレークスルーが得られたのは大きい」とたたえる。
成果の立役者となった薬学部6年生の中尾新(しん)さんは「患者さんに適用できる条件にしたかった。pH9ではその土俵に立てないので、pH7でもやった。たまたまの成功だが、やってよかった」と控え目に振り返る。
SDGsを重要指針に
須藤教授は「光を薬にする」をコンセプトに、ロドプシンの研究を続けている。「光は全ての生命活動のエネルギーの源で、毎日浴びている。光が薬になれば例えば、先進国も途上国も関係なく活用できる」。国連のSDGs(持続可能な開発目標)を重要指針とし、特に3番「全ての人に健康と福祉を」、7番「エネルギーをみんなにそしてクリーンに」、10番「人や国の不平等をなくそう」を強く意識しているという。
18~19世紀の大詩人ゲーテは、臨終に「Mehr Licht!(もっと光を!)」と語ったという。その真意はともかく、再生可能エネルギー、光触媒、光通信といった現代の技術のキーワードを聞くにつけ、この言葉が頭に浮かぶ。医療も含め、人類には課題解決のため、「もっと光を」味方につける余地がありそうだ。
関連リンク
- 岡山大学などプレスリリース「光で狙った細胞を死滅させる新技術の開発 副作用のない光がん治療法に向けて」




