流行語にもなったメタボリックシンドローム※1(通称メタボ)は、今ではすっかり定着し、おなかぽっこり体型の代名詞となった。しかし、メタボは見た目のかっこ悪さを警告しているのではない。そのおなかについた「内臓脂肪」がさまざまな生活習慣病の引き金となり、死を早めてしまう。内臓脂肪がいったいどんな悪さをするのだろう。慶應義塾大学の研究チームは、私たちの体を外敵から守る免疫システムに着目し、内臓脂肪が病気を引き起こすメカニズムを解明しようとしている。
※1 メタボリックシンドローム/内臓脂肪の過剰蓄積に加え、高脂血症、高血糖、高血圧などの条件がそろった状態。
内臓脂肪はどうしてたまる?
私たちの体は、食べ物から摂ったエネルギーを使いきれなかったとき、それを脂肪に換えて体に蓄え、必要なときにもう一度エネルギーに換えて使うことができる。進化の過程で厳しい生存競争を勝ち抜くために、なくてはならなかった素晴らしいシステムだ。しかし、美味しいものがあふれ、それほど体を動かさなくても暮らしていける現代では、皮肉にも脂肪のためこみすぎが問題となっている。
蓄える脂肪には、内臓脂肪と皮下脂肪がある。内臓脂肪は、腸間膜(ちょうどおへそあたりで小腸を支えている膜)に蓄えられる脂肪のことだ。 余ったエネルギーは、まず内臓脂肪に、そして皮下脂肪に蓄えられる。逆にエネルギー不足のときには内臓脂肪が先にエネルギー源として使われるので、内臓脂肪はつきやすくとれやすいタイプの脂肪と言われている。一般に、内臓脂肪は女性に比べて男性につきやすい。女性は、女性ホルモンの影響で、内臓脂肪よりも太ももやお尻などに皮下脂肪がつきやすいのだ。
内臓脂肪はなぜ悪い?
皮下脂肪と比べ、内臓脂肪は深刻な病気との関わりがあるとして問題視されている。 糖尿病、心筋梗塞、脳卒中、心不全がその代表的な病気だ。前述したが、内臓脂肪はつきやすくとれやすい、つまり合成も分解も盛んなので、内臓脂肪がたくさんつくと、その分多くの脂肪が分解され、血液中に流れ出す。高脂血症の状態だ。これが動脈硬化を進め、病気を引き起こす。
また、内臓脂肪の組織に炎症が起き、それが全身に広がって慢性炎症が起こり、病気のリスクが高まることも分かっている。炎症は、体が、外敵や死んでしまった自分の細胞を取り除いて自分を守ろうとする免疫反応だ。急性炎症を大火事に例えるなら、慢性炎症は体のあちらこちらでぼやが絶えず起きているような感じだ。
内臓脂肪と老化の意外な共通点
慢性炎症は、内臓脂肪の多い少ないにかかわらず、高齢者に特徴的な症状のひとつでもある。歳をとると免疫が老化して、炎症が起こりやすくなるのだ。近年解明されたそのメカニズムは非常に興味深い。
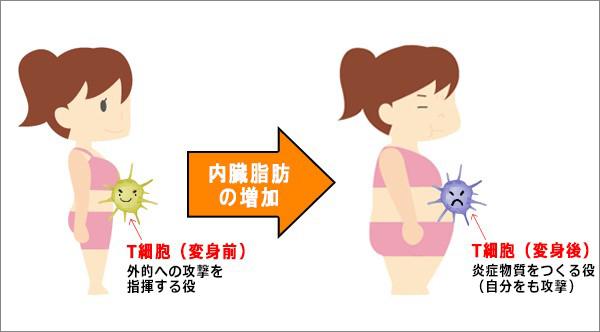
免疫システムを担うのは、白血球を中心としたさまざまな種類の免疫細胞だ。それぞれに役割があり(例えば、外敵を見つける役、攻撃する役、攻撃を指揮する役など)、チームで働いている。ところが歳をとると、本来は攻撃を指揮する役の「Tリンパ球」という免疫細胞(以下、T細胞)が、外敵を攻撃する武器(炎症物質)をつくる役に姿を変え、チームをのっとってしまう。炎症物質は血液中を流れて全身を巡り、体に炎症を起こりやすくする。
この加齢に伴う免疫の老化が、なんと内臓脂肪型肥満の体内でも起こることが、佐野元昭(さの もとあき)慶應義塾大学医学部教授率いる研究チームの行ったマウス実験で確認された。次にその実験を紹介しよう。
見えてきた真犯人
実験は、若いマウスを脂肪の多い餌で太らせ、内臓脂肪型肥満の状態にし、その免疫細胞を調べるというものだ。マウスの体重をどんどん増やしていき、高脂肪の餌を食べ始めて3?4カ月もすると、蓄積された内臓脂肪の炎症ばかりでなく、血糖値を下げるインスリンの効きが悪くなるインスリン抵抗性も発症した。
このときのマウスの免疫細胞を調べると、若いマウスが本来持つはずのない老化したT細胞が激増していたのだ。加齢による免疫の老化と同じ現象だ。研究チームは、その老化したT細胞がつくる炎症物質「オステオポンチン」に着目した。オステオポンチンは、骨をはじめとする体のさまざまな組織や血液、尿にも存在するタンパク質だ。骨を形成したり、傷を修復したり、体にとって欠かせない役割を果たす一方で、がんの進行にも関わっているとして今注目されている物質だ。
研究チームはいくつかの条件で実験を行い、オステオポンチンが内臓脂肪の炎症やインスリン抵抗性を引き起こしていることをつきとめた。まず、健康なマウスに老化したT細胞を移植すると、オステオポンチンがつくられ、やはり同じように悪さをした。しかし、移植する老化したT細胞が遺伝的にオステオポンチンをつくれないマウス由来だった場合、 内臓脂肪の炎症やインスリン抵抗性は起きなかったのだ。
さらに、オステオポンチンが引き起こす炎症は、歯止めがきかないことも分かった。通常、炎症が起きると、それをストップさせるために免疫のブレーキがかかるのだが、老化したT細胞がオステオポンチンをつくる炎症反応には、このブレーキは全くかからない。オステオポンチンが強力な炎症物質であることを裏付ける結果だ。
成果から見えてきたもの
内臓脂肪型肥満に伴う慢性炎症の機序(からくり)については、これまでにも示唆に富む研究成果が多くあり、佐野さんのグループでも再現してきた。「その機序の悪の指揮者を発見したことになるのでは…」と佐野さんは今回の成果を振り返る。
それは、内臓脂肪型肥満が引き起こす症状や病気をくいとめるための治療法開発の道が見えてきたことを意味する。その治療法では、「老化したT細胞を選択的に体内から排除すること」がポイントになる。佐野さんはこう話す。
「この方法が分かれば、肥満だけでなく高齢者の慢性炎症を制御して、健康長寿の実現に貢献できるかもしれません。脳卒中や心不全、血管病に加え、がん、COPD、CKD、サルコペニア※2、認知機能低下に対しても予防効果を発揮する可能性が期待できると思います」
※2 COPD、CKD、サルコペニア/COPDは慢性閉塞性肺疾患、CKDは慢性腎臓病、サルコペニアは筋肉量の低下を招く病気。
新しい治療法開発は、今後の研究テーマになっていくだろう。そして、もしそれが誕生しても、やはり「太らないこと」が治療の大前提だ。しかし、太って老化してしまったT細胞は、痩せたら若返るだろうか。これについては今研究中だという。尽きない研究テーマに、医学、そして私たちの体に備わるさまざまなメカニズムの複雑さを感じる。
「医学では、まだ病態の理解が不十分の領域が多々あります。特に循環器病領域は、病態の理解が遅れていて、対症療法にとどまっています。原因療法が存在しないのが現実です。われわれの研究が、将来、病態の解明や原因療法の確立に役立てればと思い研究を続けています」。そう語る佐野さんが感じている研究の魅力は、「今まで分からなかったものが分かるようになること」。そんなシンプルな思いが、複雑な病態のメカニズムをも、確実に解明へと導いていくように感じた。
おわりに
今日本でメタボリックシンドロームが疑われる人は、予備軍を含めると、男性の約半数、女性の約20パーセントに及ぶ。その割合は、男性では40歳以降、女性では60歳以降にぐんと増える。(平成26年度国民健康・栄養調査報告より)内臓脂肪型肥満の新しい治療法が確立されれば、これらの人が実際に病気を発症するのを食い止め、寿命は延びるかもしれない。だからといって、安心して不自然な生活習慣を続けていいわけではないだろう。革新的な医学の進歩と、私たち自らが心がける予防とで、真の健康寿命の延伸を目指したい。
(サイエンスライター 丸山 恵)




